引用本文: 胡旭, 董吉榮, 徐鳳, 李曉玉, 孫詩白. 正電子發射計算機斷層顯像-核磁共振成像影像融合輔助下腦囊蟲病致癲癇的外科治療一例. 癲癇雜志, 2021, 7(1): 81-83. doi: 10.7507/2096-0247.20210014 復制
腦囊蟲病(Neurocysticercosis,NCC)是由豬肉絳蟲的囊尾蚴寄生于人腦所引起的一種感染性疾病,癲癇發作是其最主要的臨床表現[1],其中腦實質型NCC癲癇發病率高達 70%~90%[2, 3]。近 20% 患者通過驅蟲藥物治療仍無法控制癲癇發作[4],隨著影像后處理技術的不斷發展,正電子發射計算機斷層顯像-核磁共振成像(PET-MRI)影像融合技術可輔助確定手術切除范圍,從而提高癲癇的治愈率。現報道一例腦實質型NCC患者,通過 PET-MRI 融合明確手術切除范圍后切除致癇灶,取得了良好的治療效果。
臨床資料 患者 女,24 歲,右利手。因“反復四肢抽搐伴意識障礙 4 年”入院,患者有兩種發作形式:第一種表現為突發四肢抽搐,意識喪失,牙關緊閉,每次持續約 2~3 min,發作頻率為每年 1~2 次;第二種表現為意識喪失,咀嚼、吞咽動作,左側上肢摸索或整理動作,每次持續約 1~2 min,發作頻率為 1~2 次/月。曾于外院就診,診斷為“癲癇”,給予口服奧卡西平 300 mg 每日三次、托吡酯 50 mg 每日兩次,效果不佳。入院后主訴平日有頭痛,睡眠質量差并多夢,感記憶力下降,有似曾相識感,偶爾可聞到奇怪臭味。曾在內蒙古居住 4 年,既往無熱性驚厥史、無癲癇持續狀態史、無外傷史、出生正常,家族中無癲癇病史。
神經系統查體:意識清楚,精神可,GCS評分15 分,顱神經檢查無異常,頸軟,無抵抗,四肢深淺感覺及復合感覺正常,四肢肌力﹑肌張力及肌容量正常,無不自主運動,共濟運動均正常,雙側肱二頭肌﹑跟﹑膝腱反射正常,兩側 Babinski 征(?)、Chardock 征(?)、Openheim 征(?)、Gordon 征(?)。
術前評估相關檢驗及檢查:血常規:白細胞 3.26×109/L(正常值:4.0×109/L~10.0×109/L),中性細胞數 1.38×109/L(正常值:2.0×109/L~7.0×109/L),淋巴細胞比率 0.466(正常值:0.2~0.4)。腰椎穿刺術:腦壓 120 mmHg,腦脊液無色透明,有核細胞數 8.5×106/L,囊蟲抗體陽性。頭部 MRI(平掃+增強)示:左側顳葉內側可見分葉狀長 T1 長 T2 信號影,DWI 呈低信號,大小約 1.5 cm×1.5 cm,T2 FLAIR 序列病灶周圍腦組織見輕度水腫帶,其內可見分隔,增強后囊壁及其內分隔輕度強化。長程視頻腦電圖(VEEG)示:未捕捉到發作;發作間期可見各導聯 θ 波增多,左側顳區及蝶骨電極見中高幅 1.5~2.0 Hz 尖慢波頻繁單發,左側蝶骨電極顯著。頭部 PET 示:左側顳葉內側低代謝改變。通過 MATLAB 及 spm 軟件,將 PET 與 MRI 進行影像融合后提示,左側顳葉內側及顳上回前部低代謝改變。神經心理學評估:蒙特利爾認知評估基礎量表(MOCA-B)、簡易智能狀態檢查(MMSE)均正常。患者病程各階段影像學及術后病理學檢查見圖 1~4。
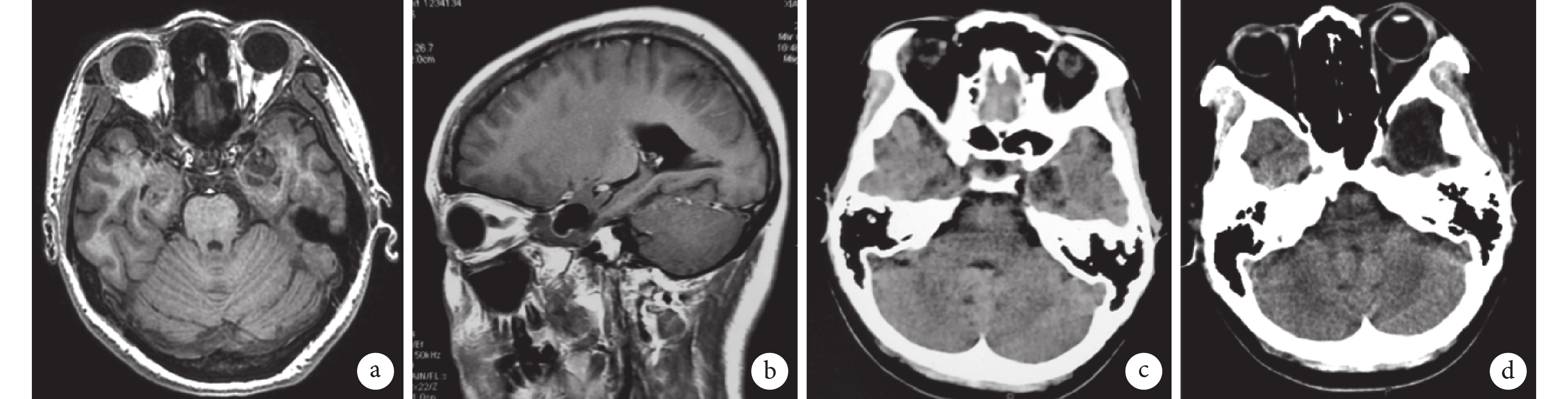 圖1
患者頭部 MRI 及 CT
圖1
患者頭部 MRI 及 CT
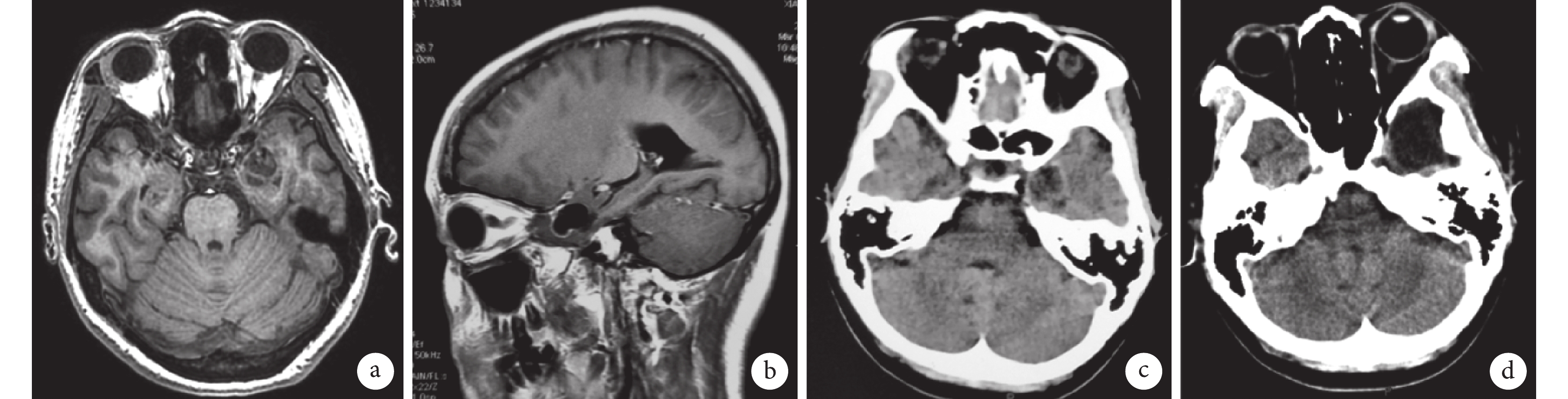
a. MRI T1 平掃:分葉狀長 T1 信號影;b. MRI T1 增強:囊壁及其內分隔輕度強化;c. 術前 CT;d. 術后 CT
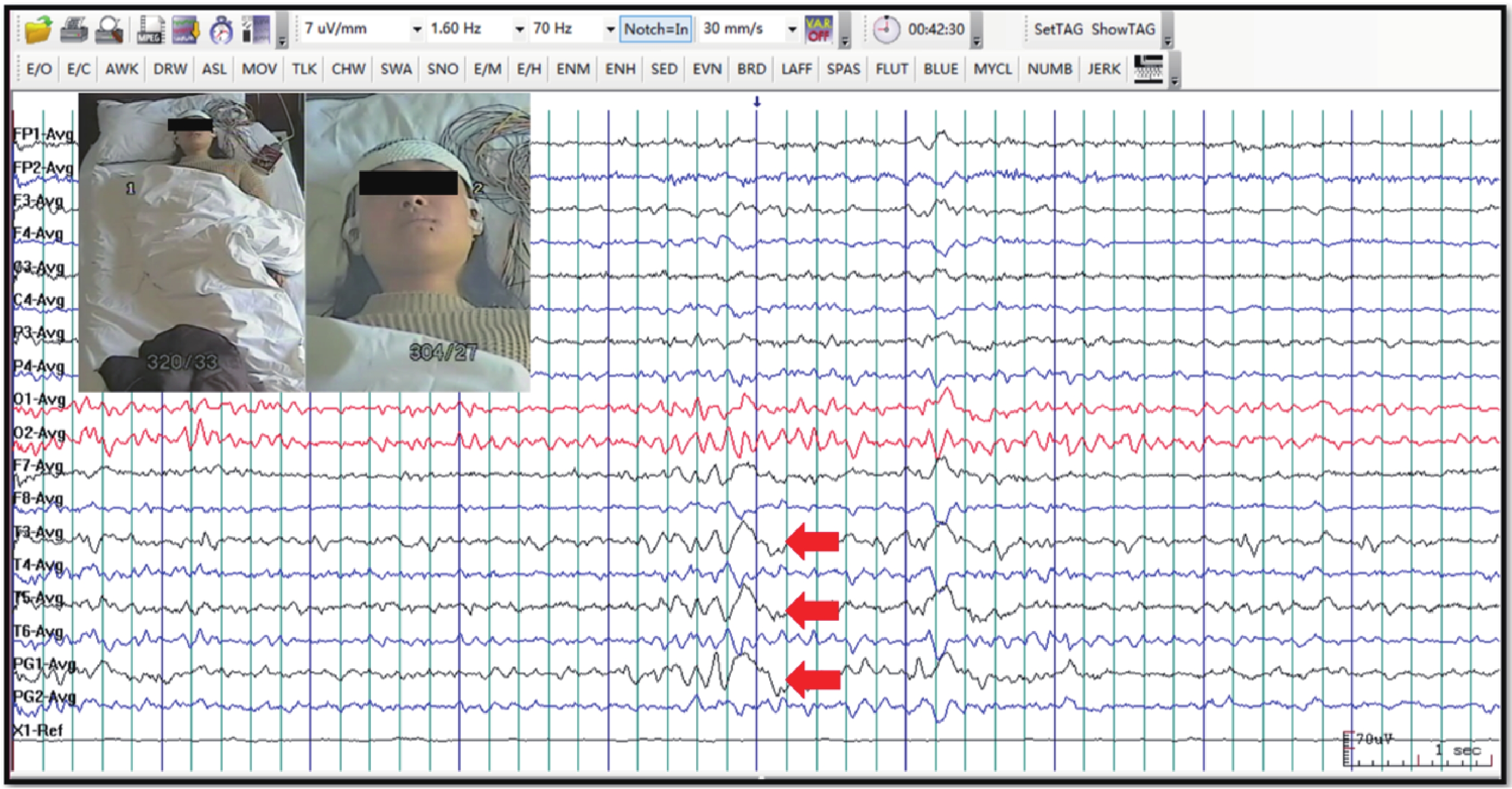 圖2
患者 VEEG
圖2
患者 VEEG
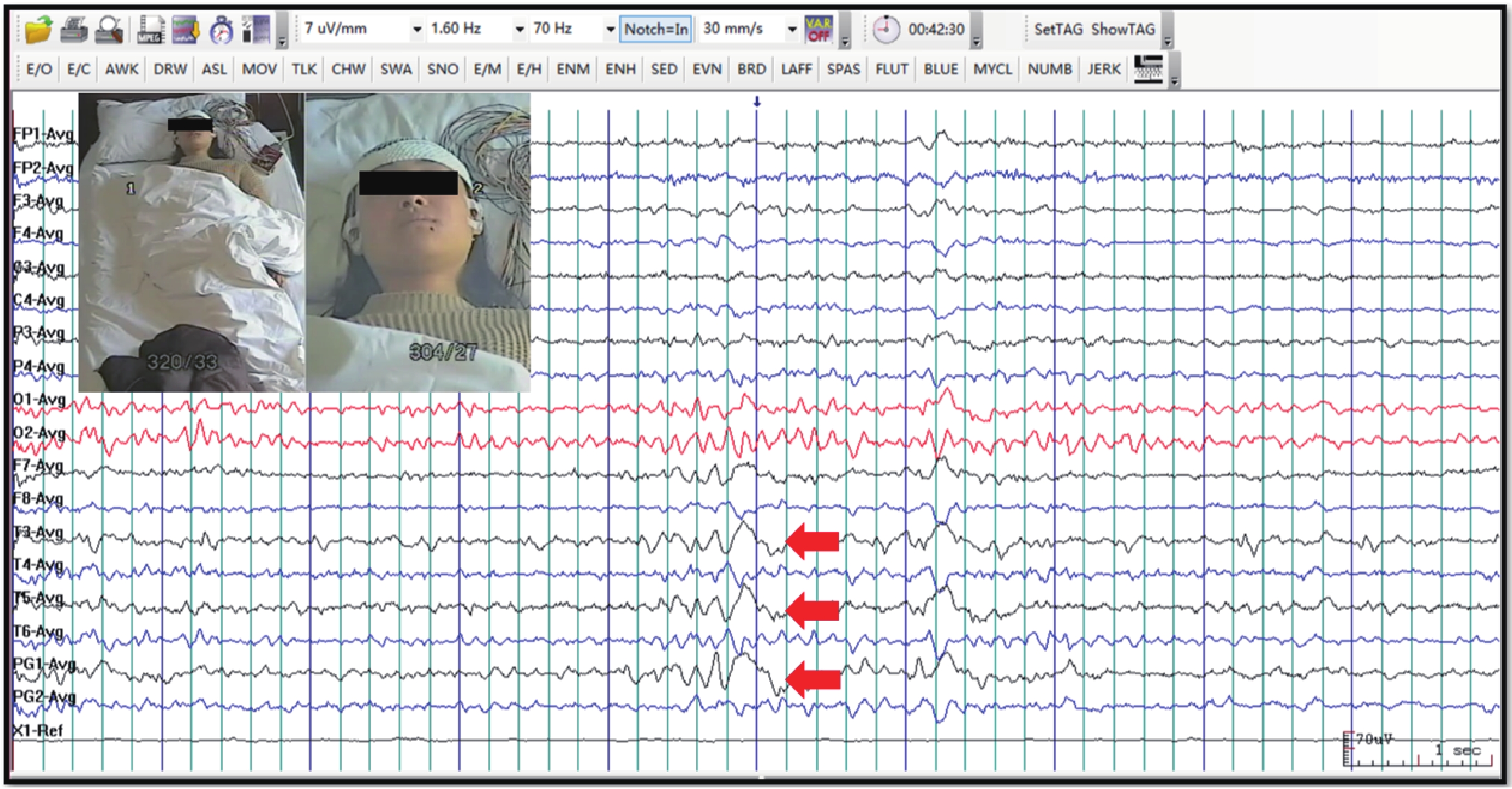
左側顳區及蝶骨電極見尖慢波頻繁單發(箭頭)
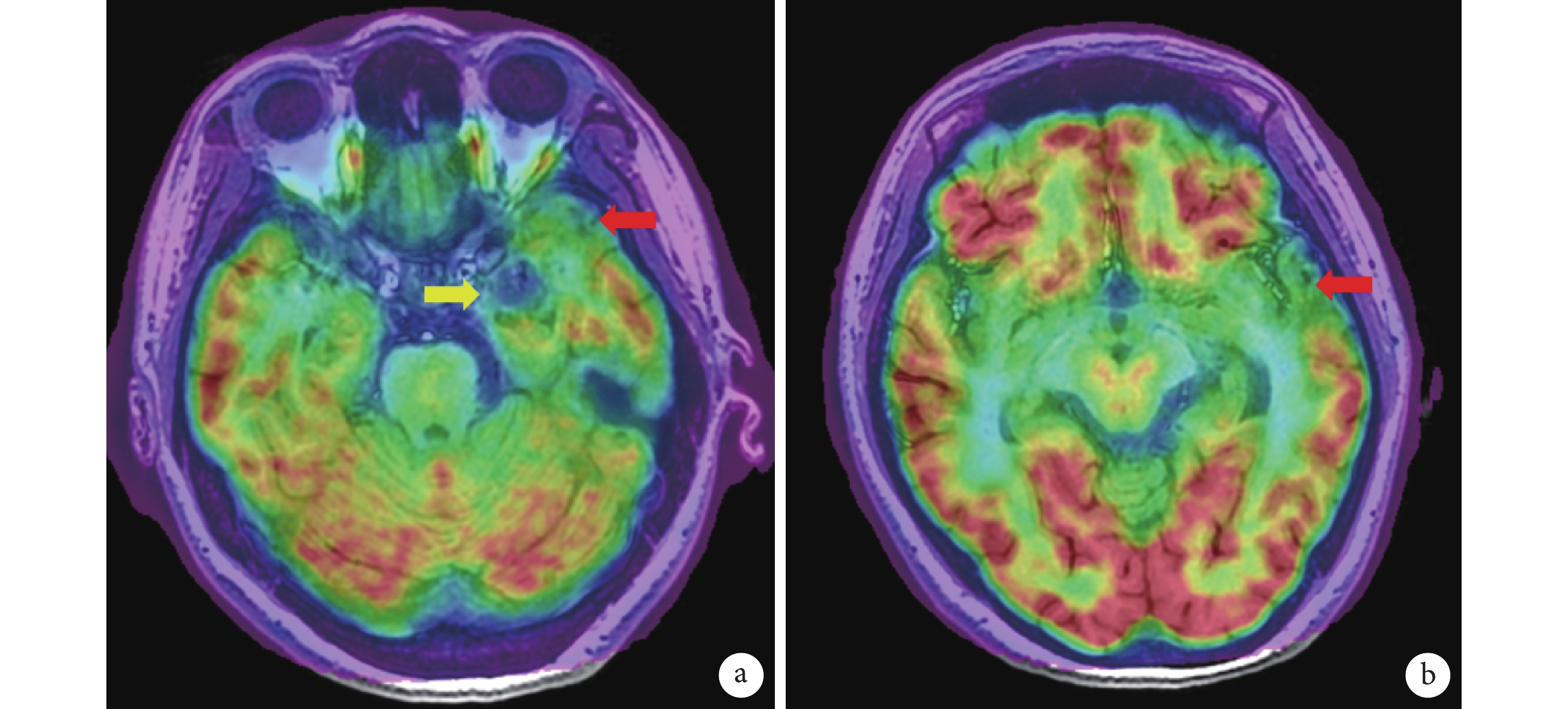 圖3
患者頭部 PET-MRI 影像融合
圖3
患者頭部 PET-MRI 影像融合
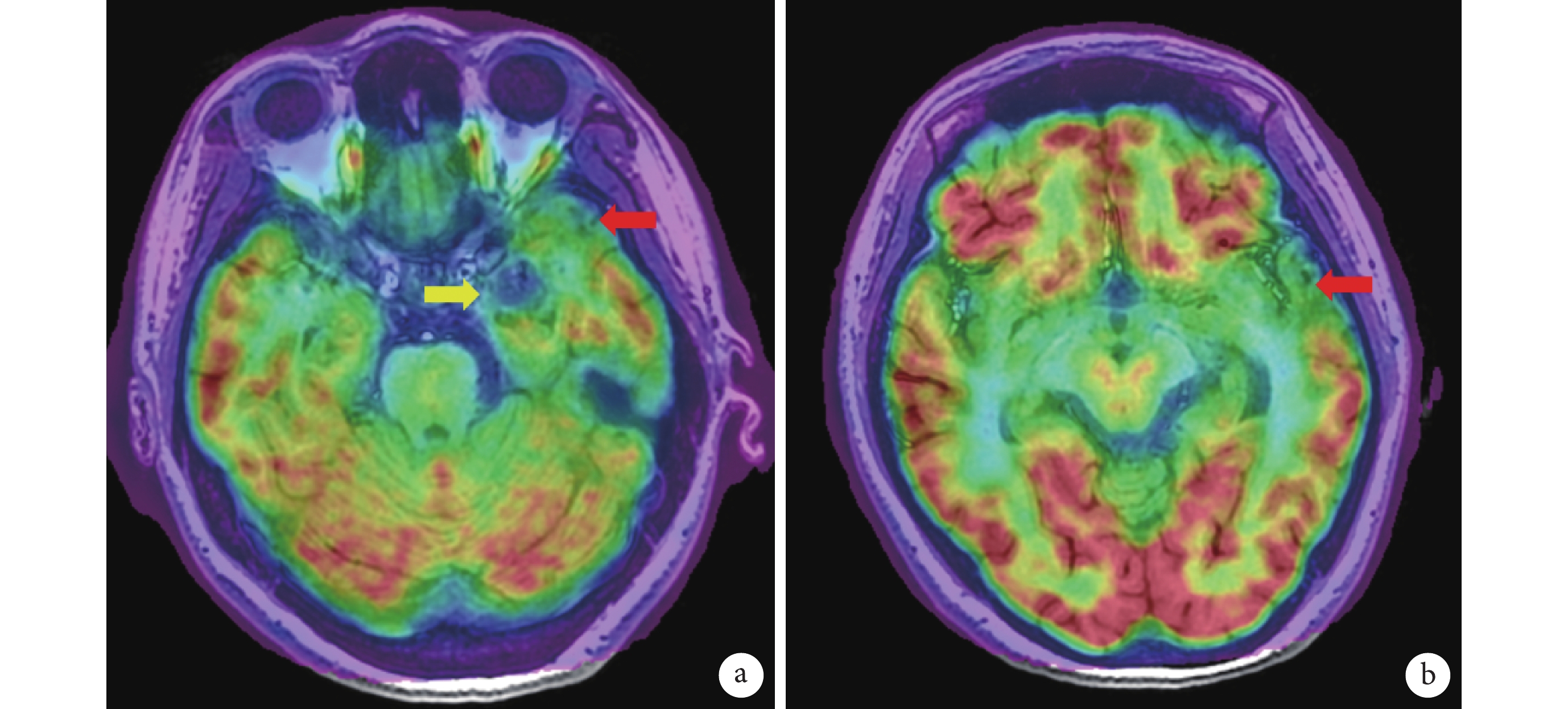
左側顳葉內側病變(黃色箭頭)、顳上回前部低代謝(紅色箭頭)
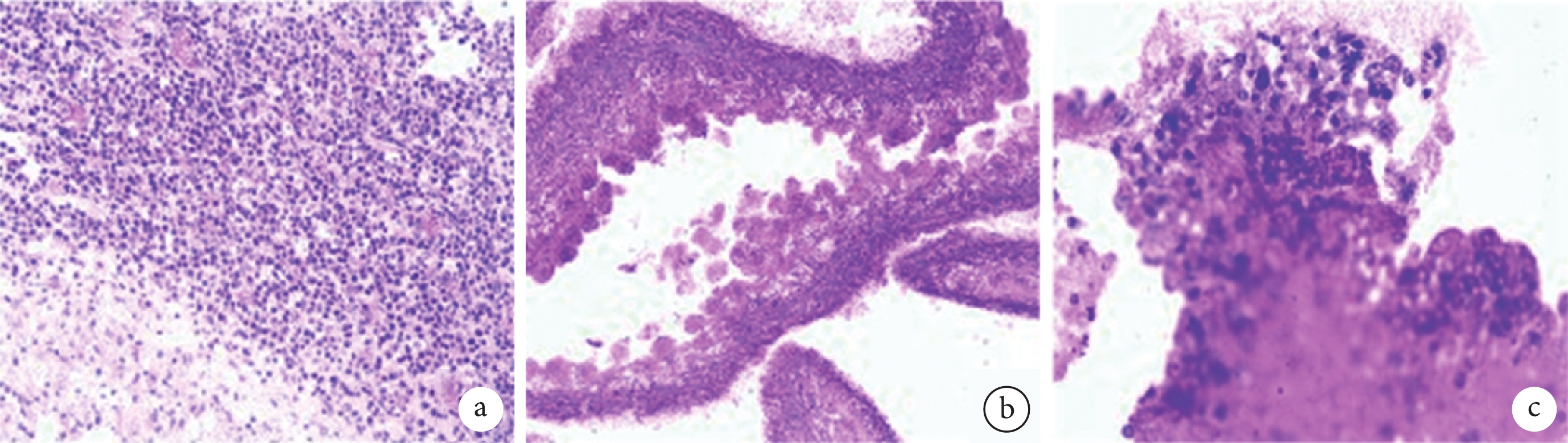 圖4
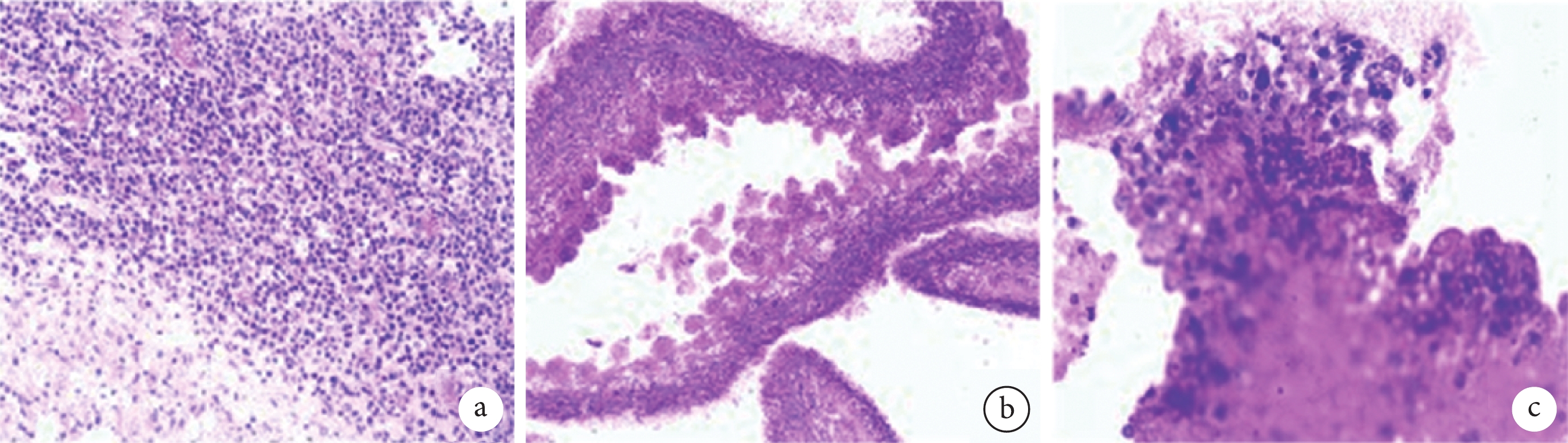
患者術后病理檢查(HE 染色,補充放大倍數)
圖4
患者術后病理檢查(HE 染色,補充放大倍數)
a. 腦組織及增生血管和膠質,淋巴漿細胞浸潤,組織細胞反應;b. 寄生蟲,蟲體表面呈鋸齒狀;c. 體腔內見體細胞
治療經過 根據患者腦脊液檢查提示囊蟲抗體陽性,頭部 MRI 提示左側顳葉內側分葉狀長 T1 長 T2 信號影,增強后囊壁及其內分隔輕度強化,且癲癇發作頻率為每月 1~2 次。診斷為NCC;難治性癲癇。鑒于患者發作較頻繁,及患者家屬意愿,給予手術治療。手術擬切除范圍為囊蟲病灶及 PET-MRI 影像融合顯示的顳上回前部低代謝區域。術中見左側顳上回皮層萎縮,硬腦膜與腦表面有血管黏連,術中皮層及深部電極檢測提示,左側顳上回前部皮層及顳葉內側癲癇樣放電明顯,與術前 PET-MRI 影像融合后低代謝范圍相同,切除顳葉前部及顳葉內側病灶。術后病理:豬囊蟲病。囊壁切片示腦組織及增生血管和膠質,大量淋巴漿細胞浸潤,組織細胞反應,另見寄生蟲,蟲體表面呈鋸齒狀,體腔內見體細胞。術后給予口服吡喹酮驅蟲治療,目前隨訪 1 年無癲癇發作。
討論 NCC占囊蟲病的 60%~90%,屬于顱內感染性疾病之一,主要與吃生豬肉、生菜、砧板生熟不分等不良衛生習慣相關[5, 6]。以東北、華北地區多見,西北地區及云南次之[7]。該患者有在內蒙古居住 4 年病史,患病與當地飲食及衛生防病知識的匱乏有關。
根據NCC的臨床表現可分為癲癇型、腦膜炎型、顱內壓增高型、脊髓型及癡呆型,其中以癲癇發作為最突出癥狀[8]。癲癇發作形式與囊尾蚴寄生的部位密切相關,發作頻率與周圍腦組織炎性的免疫反應有關[9, 10]。單病灶引起的癲癇以部分性發作為主,而多病灶引起的癲癇絕大多數以全身發作為主,且可有兩種以上的發作形式。
治療方法包括抗病原學治療和囊蟲病灶切除手術。在抗囊蟲治療的早期,由于囊蟲崩裂死亡較多,毒素刺激及炎性反應較重,可能誘發癲癇發做更加頻繁,程度更重,且驅蟲后有近 20% 的病灶不能吸收,導致癲癇繼續發作[4]。有學者認為單發囊蟲摘除后癲癇控制不佳[11],我們認為,效果不佳的原因為導致癲癇發作的范圍可能大于囊蟲病灶的范圍,單純切除囊蟲病灶而未能完整切除致癇灶。該患者臨床癥狀學、EEG 發作間期及頭部 MRI 提示為左側內側顳葉起源,行 PET-MRI 影像融合后提示,左側顳葉內側及顳上回前部低代謝改變。術中見左顳上回皮層萎縮,術中皮層電極提示顳上回癲癇樣放電,說明致癇灶與 PET-MRI 影像融合顯示低代謝范圍相吻合,切除致癇灶后無癲癇發作。
PET-CT 對定位致癇灶有敏感性及特異性高等優點,MRI 可清晰顯示解剖結構,將 PET 與 MRI 影像融合后定位致癇灶更加準確。有文獻報道,使用 PET-MRI 對癲癇患者進行術前評估,可改善患者預后[12]。囊尾蚴在腦內寄生的過程中可釋放大量的抗原和毒素,導致致癇灶的范圍遠大于囊蟲病灶的范圍,術前通過 PET-MRI 影像融合可有效確定手術切除范圍。建議,對于臨床上癲癇發作頻繁的單發NCC患者可直接行手術治療,關鍵在于確定致癇灶的范圍。
腦囊蟲病(Neurocysticercosis,NCC)是由豬肉絳蟲的囊尾蚴寄生于人腦所引起的一種感染性疾病,癲癇發作是其最主要的臨床表現[1],其中腦實質型NCC癲癇發病率高達 70%~90%[2, 3]。近 20% 患者通過驅蟲藥物治療仍無法控制癲癇發作[4],隨著影像后處理技術的不斷發展,正電子發射計算機斷層顯像-核磁共振成像(PET-MRI)影像融合技術可輔助確定手術切除范圍,從而提高癲癇的治愈率。現報道一例腦實質型NCC患者,通過 PET-MRI 融合明確手術切除范圍后切除致癇灶,取得了良好的治療效果。
臨床資料 患者 女,24 歲,右利手。因“反復四肢抽搐伴意識障礙 4 年”入院,患者有兩種發作形式:第一種表現為突發四肢抽搐,意識喪失,牙關緊閉,每次持續約 2~3 min,發作頻率為每年 1~2 次;第二種表現為意識喪失,咀嚼、吞咽動作,左側上肢摸索或整理動作,每次持續約 1~2 min,發作頻率為 1~2 次/月。曾于外院就診,診斷為“癲癇”,給予口服奧卡西平 300 mg 每日三次、托吡酯 50 mg 每日兩次,效果不佳。入院后主訴平日有頭痛,睡眠質量差并多夢,感記憶力下降,有似曾相識感,偶爾可聞到奇怪臭味。曾在內蒙古居住 4 年,既往無熱性驚厥史、無癲癇持續狀態史、無外傷史、出生正常,家族中無癲癇病史。
神經系統查體:意識清楚,精神可,GCS評分15 分,顱神經檢查無異常,頸軟,無抵抗,四肢深淺感覺及復合感覺正常,四肢肌力﹑肌張力及肌容量正常,無不自主運動,共濟運動均正常,雙側肱二頭肌﹑跟﹑膝腱反射正常,兩側 Babinski 征(?)、Chardock 征(?)、Openheim 征(?)、Gordon 征(?)。
術前評估相關檢驗及檢查:血常規:白細胞 3.26×109/L(正常值:4.0×109/L~10.0×109/L),中性細胞數 1.38×109/L(正常值:2.0×109/L~7.0×109/L),淋巴細胞比率 0.466(正常值:0.2~0.4)。腰椎穿刺術:腦壓 120 mmHg,腦脊液無色透明,有核細胞數 8.5×106/L,囊蟲抗體陽性。頭部 MRI(平掃+增強)示:左側顳葉內側可見分葉狀長 T1 長 T2 信號影,DWI 呈低信號,大小約 1.5 cm×1.5 cm,T2 FLAIR 序列病灶周圍腦組織見輕度水腫帶,其內可見分隔,增強后囊壁及其內分隔輕度強化。長程視頻腦電圖(VEEG)示:未捕捉到發作;發作間期可見各導聯 θ 波增多,左側顳區及蝶骨電極見中高幅 1.5~2.0 Hz 尖慢波頻繁單發,左側蝶骨電極顯著。頭部 PET 示:左側顳葉內側低代謝改變。通過 MATLAB 及 spm 軟件,將 PET 與 MRI 進行影像融合后提示,左側顳葉內側及顳上回前部低代謝改變。神經心理學評估:蒙特利爾認知評估基礎量表(MOCA-B)、簡易智能狀態檢查(MMSE)均正常。患者病程各階段影像學及術后病理學檢查見圖 1~4。
 圖1
患者頭部 MRI 及 CT
圖1
患者頭部 MRI 及 CT
a. MRI T1 平掃:分葉狀長 T1 信號影;b. MRI T1 增強:囊壁及其內分隔輕度強化;c. 術前 CT;d. 術后 CT
 圖2
患者 VEEG
圖2
患者 VEEG
左側顳區及蝶骨電極見尖慢波頻繁單發(箭頭)
 圖3
患者頭部 PET-MRI 影像融合
圖3
患者頭部 PET-MRI 影像融合
左側顳葉內側病變(黃色箭頭)、顳上回前部低代謝(紅色箭頭)
 圖4
患者術后病理檢查(HE 染色,補充放大倍數)
圖4
患者術后病理檢查(HE 染色,補充放大倍數)
a. 腦組織及增生血管和膠質,淋巴漿細胞浸潤,組織細胞反應;b. 寄生蟲,蟲體表面呈鋸齒狀;c. 體腔內見體細胞
治療經過 根據患者腦脊液檢查提示囊蟲抗體陽性,頭部 MRI 提示左側顳葉內側分葉狀長 T1 長 T2 信號影,增強后囊壁及其內分隔輕度強化,且癲癇發作頻率為每月 1~2 次。診斷為NCC;難治性癲癇。鑒于患者發作較頻繁,及患者家屬意愿,給予手術治療。手術擬切除范圍為囊蟲病灶及 PET-MRI 影像融合顯示的顳上回前部低代謝區域。術中見左側顳上回皮層萎縮,硬腦膜與腦表面有血管黏連,術中皮層及深部電極檢測提示,左側顳上回前部皮層及顳葉內側癲癇樣放電明顯,與術前 PET-MRI 影像融合后低代謝范圍相同,切除顳葉前部及顳葉內側病灶。術后病理:豬囊蟲病。囊壁切片示腦組織及增生血管和膠質,大量淋巴漿細胞浸潤,組織細胞反應,另見寄生蟲,蟲體表面呈鋸齒狀,體腔內見體細胞。術后給予口服吡喹酮驅蟲治療,目前隨訪 1 年無癲癇發作。
討論 NCC占囊蟲病的 60%~90%,屬于顱內感染性疾病之一,主要與吃生豬肉、生菜、砧板生熟不分等不良衛生習慣相關[5, 6]。以東北、華北地區多見,西北地區及云南次之[7]。該患者有在內蒙古居住 4 年病史,患病與當地飲食及衛生防病知識的匱乏有關。
根據NCC的臨床表現可分為癲癇型、腦膜炎型、顱內壓增高型、脊髓型及癡呆型,其中以癲癇發作為最突出癥狀[8]。癲癇發作形式與囊尾蚴寄生的部位密切相關,發作頻率與周圍腦組織炎性的免疫反應有關[9, 10]。單病灶引起的癲癇以部分性發作為主,而多病灶引起的癲癇絕大多數以全身發作為主,且可有兩種以上的發作形式。
治療方法包括抗病原學治療和囊蟲病灶切除手術。在抗囊蟲治療的早期,由于囊蟲崩裂死亡較多,毒素刺激及炎性反應較重,可能誘發癲癇發做更加頻繁,程度更重,且驅蟲后有近 20% 的病灶不能吸收,導致癲癇繼續發作[4]。有學者認為單發囊蟲摘除后癲癇控制不佳[11],我們認為,效果不佳的原因為導致癲癇發作的范圍可能大于囊蟲病灶的范圍,單純切除囊蟲病灶而未能完整切除致癇灶。該患者臨床癥狀學、EEG 發作間期及頭部 MRI 提示為左側內側顳葉起源,行 PET-MRI 影像融合后提示,左側顳葉內側及顳上回前部低代謝改變。術中見左顳上回皮層萎縮,術中皮層電極提示顳上回癲癇樣放電,說明致癇灶與 PET-MRI 影像融合顯示低代謝范圍相吻合,切除致癇灶后無癲癇發作。
PET-CT 對定位致癇灶有敏感性及特異性高等優點,MRI 可清晰顯示解剖結構,將 PET 與 MRI 影像融合后定位致癇灶更加準確。有文獻報道,使用 PET-MRI 對癲癇患者進行術前評估,可改善患者預后[12]。囊尾蚴在腦內寄生的過程中可釋放大量的抗原和毒素,導致致癇灶的范圍遠大于囊蟲病灶的范圍,術前通過 PET-MRI 影像融合可有效確定手術切除范圍。建議,對于臨床上癲癇發作頻繁的單發NCC患者可直接行手術治療,關鍵在于確定致癇灶的范圍。